Isótopos Radiactivos
 Para comprender la Química Nuclear y sus reacciones, debemos recordar el concepto de Isótopo, ¿Recuerdas que era un Isótopo?
Para comprender la Química Nuclear y sus reacciones, debemos recordar el concepto de Isótopo, ¿Recuerdas que era un Isótopo?A ver, recordemos un poco, existe 3 tipos de Nuclidos: Isótonos, Isóbaros e Isótopos. Para comprender esto, partamos definiendo que significa el prefijo "Iso" hace referencia a una igualdad. Esta igualdad acompañada por un sufijo, ya sea "tonos", "baros" o "topos".
- Los Isótonos, son átomos que tienen igual número de neutrones, sin embargo, estos difieren en su número másico(A).
- Los Isóbaros, son átomos que tienen igual número másico(A), sin embargo, estos diferenten en el número atómico o cantidad de protones(Z).
- Los Isótopos, son átomos que tienen igual número atómico o de protones (Z), sin embargo, estos difieren en su número másico(A).
A CONTINUACIÓN, TE PRESENTO UNA ESTRATEGÍA DE APRENDIZAJE PARA APRENDER CON MAYOR FACILIDAD ESTOS CONCEPTOS.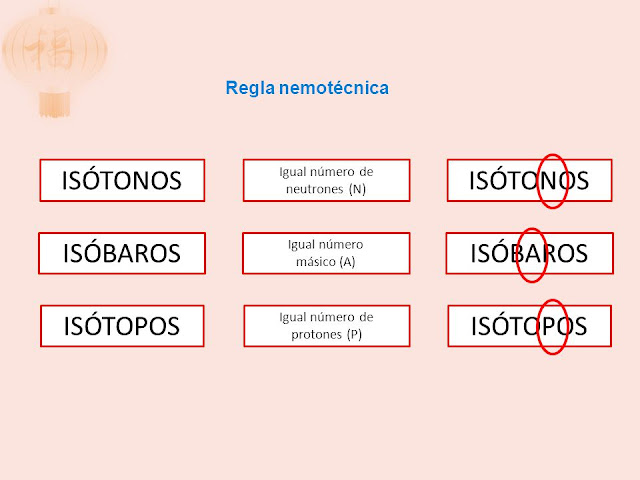
EJEMPLOS: DENTRO DE DEL CAMPO DE LA QUÍMICA NUCLEAR, LOS ELEMENTOS CON NÚMERO ATÓMICO MAYOR A 83 (Z>83), SERÁN RADIACTIVOS, POR LO TANTO, SU NÚCLEOS SON INESTABLES Y ESTOS EMITIRÁN RADIACIONES DE MANERA ESPONTÁNEA.
DENTRO DE DEL CAMPO DE LA QUÍMICA NUCLEAR, LOS ELEMENTOS CON NÚMERO ATÓMICO MAYOR A 83 (Z>83), SERÁN RADIACTIVOS, POR LO TANTO, SU NÚCLEOS SON INESTABLES Y ESTOS EMITIRÁN RADIACIONES DE MANERA ESPONTÁNEA.
UN EJEMPLO DE ELLO, ES EL ISÓTOPO RADIACTIVO (ISÓTOPO CON Z>83), ES EL URANIO 238 Y 235 (NÚMEROS QUE HACEN REFERENCIA A SU NÚMERO MÁSICO), ESTOS POSEEN IGUAL Z (92), PERO DISTINTA CANTIDAD DE NEUTRONES, POR LO TANTO, DIFIEREN EN SU NÚMERO MÁSICO.

Si aún por tu cabeza rondan preguntas como ¿Qué era entonces un isótopo radiactivo?, no te preocupes, probablemente tenga una solución, a continuación te dejo un vídeo para que logres comprender de mejor forma la idea que te he intentado transmitir durante este post. ¡Ponte cómodo, prepara tus neuronas y ve por un cuaderno y un lápiz para anotar un par de apuntes!
VIDEO ISÓTOPOS:
IMPORTANTE : SI NO RECUERDAS CÓMO CÁLCULAR LA CANTIDAD DE PROTONES, NEUTRONES Y ELECTRONES, PUEDES IR A LA SECCIÓN DE "REPASO DE PARTÍCULAS SUBATÓMICAS", AHÍ CONOCERÁS LOS CONCEPTOS Y LAS FORMAS DE CÁLCULAR DICHAS PARTÍCULAS.

Comentarios
Publicar un comentario